为进一步推进保健食品备案工作,根据《中华人民共和国食品安全法》,市场监管总局组织制修订了人参等三种保健食品原料目录(征求意见稿),现面向社会公开征求意见,意见建议反馈截止时间为2022年11月25日。公众可以通过以下途径和方式提出意见建议:
一、登陆市场监管总局网站(网址:http://www.samr.gov.cn),通过首页“互动”栏目中的“征集调查”提出意见。
二、通过电子邮件将意见建议发送至:bjspba@cfe-samr.org.cn,邮件主题请注明“人参等三种保健食品原料目录(征求意见稿)公开征集意见”字样。
三、将意见建议邮寄至:北京市西城区北露园1号国家市场监督管理总局特殊食品司,并在信封上注明“人参等三种保健食品原料目录(征求意见稿)公开征集意见”字样。
附件:1.保健食品原料目录 人参(征求意见稿) 《 Goto人参 》
2.保健食品原料目录 西洋参(征求意见稿) 《 Goto西洋参 》
3.保健食品原料目录 灵芝(征求意见稿) 《 Goto灵芝 》
市场监管总局
2022年10月25日
《保健食品原料目录 人参(征求意见稿)》
原料名称 | 每日用量 | 功效 | |||
名称 | 用量范围 | 适宜人群 | 不适宜人群 | 注意事项 | |
人参 (人工种植,5年及以下) | 1-3g
| 易疲劳者
| 少年儿童、孕妇、乳母;湿热体质、阴虚体质者 | 不宜与含有藜芦、五灵脂的中成药同用。 感冒、舌苔厚腻、易上火者不推荐使用。 长期食用建议根据个人体质酌情减量使用。 | 缓解体力疲劳 |
免疫力低下者
| 增强免疫力 | ||||
人参原料技术要求
【来源】
人工种植5年及5年以下五加科人参属植物人参(Panax ginseng C.A. Meyer)的干燥根及根茎。
【感官要求】
应符合表 1 规定。
表 1 感官指标
项目 | 要求 |
色泽 | 全体表呈黄白色或灰黄色。断面淡黄白色 |
滋味、气味 | 香气特异,味微苦、甘。 |
状态 | 主根呈圆柱形或纺锤形,可见疏浅断续的横纹及明显的纵沟,或有支根和须根。根茎(芦头)顶端具有稀疏凹窝状茎痕(芦碗),或有不定根(艼)。无虫蛀、霉变。质地坚实、较硬。断面显粉性,形成层环纹棕黄色,皮部有黄棕色的点状树脂道及放射状裂隙面。 |
【鉴别】
1本品横切面:木栓层为数列细胞。栓内层窄。韧皮部外侧有裂隙,内侧薄壁细胞排列较紧密,有树脂道散在,内含黄色分泌物。形成层成环。木质部射线宽广,导管单个散在或数个相聚,断续排列成放射状,导管旁偶有非木化的纤维。薄壁细胞含草酸钙簇晶。
粉末淡黄白色。树脂道碎片易见,含黄色块状分泌物。草酸钙簇晶直径20〜68μm,棱角锐尖。木栓细胞表面观类方形或多角形,壁细波状弯曲。网纹导管和梯纹导管直径10〜56μm。淀粉粒甚多,单粒类球形、半圆形或不规则多角形,直径4〜20μm,脐点点状或裂缝状;复粒由2〜6分粒组成。
2取本品粉末lg,加三氯甲烷40mL,加热回流1h,弃去三氯甲烷液,药渣挥干溶剂,加水0.5mL搅拌湿润,加水饱和正丁醇10mL,超声处理30min,吸取上清液加3倍量氨试液,摇匀,放置分层,取上层液蒸干,残渣加甲醇lmL使溶解,作为供试品溶液。另取人参对照药材lg,同法制成对照药材溶液。再取人参皂苷Rb1对照品、人参皂苷Re对照品、人参皂苷Rf对照品及人参皂苷Rg1对照品,加甲醇制成每1mL各含2mg的混合溶液,作为对照品溶液。照薄层色谱法试验,吸取上述三种溶液各1〜2μ1,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15:40:22:10)10℃以下放置的下层溶液为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,分别置日光和紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱和对照品色谱相应位置上,分别显相同颜色的斑点或荧光斑点。
3取供试品粉末1g,加甲醇25mL,加热回流1h,放冷,滤过,滤液蒸干,残渣加蒸馏水20mL使溶解,用乙醚振瑶提取两次,每次10mL,弃去乙醚液,水层用水饱和的正丁醇振摇提取3次,每次15mL,合并正丁醇提取液,用水洗涤2次,每次10mL,分取正丁醇液,蒸干,残渣加甲醇1mL使溶解,作为供试品溶液。取拟人参皂苷F11对照品加甲醇制成每1mL含2mg的混合溶液,作为对照品溶液。按照(2)的方法进行薄层色谱法试验,人参中不应含拟人参皂苷F11。
【理化指标】
应符合表2规定。
表2 理化指标
项目 | 指标 | 检测方法 |
水分,% ≤ | 12.0 | GB 5009.3 |
灰分,% ≤ | 5.0 | GB 5009.4 |
铅(以Pb计),mg/kg ≤ | 0.5 | GB 5009.12 |
总砷(以As计),mg/kg ≤ | 1.0 | GB5009.11 |
总汞(以Hg计),mg/kg ≤ | 0.1 | GB 5009.17 |
镉(以Cd计), mg/kg ≤ | 0.5 | GB 5009.15 |
铜(以Cu计),mg/kg ≤ | 20 | GB 5009.13 |
二氧化硫,% ≤ | 0.05 | GB 5009.34 |
【农药残留】
应符合表3规定。
表3 农药残留指标
农药名称 | 残留物 | 最大残留量mg/kg | 检测方法 |
苯醚甲环唑 | 苯醚甲环唑 | 0.5 | GB 23200.113 |
吡唑醚菌酯 | 吡唑醚菌酯 | 0.5 | GB/T 20769(参见“百克敏”) |
丙环唑 | 丙环唑 | 0.1 | GB 23200.113 |
丁硫克百威 | 丁硫克百威 | 0.02 | GB 23200.13 |
毒虫畏 | 毒虫畏(E型和Z型异构体之和 | 0.01 | SN/T 2324 |
氟吡菌胺 | 氟吡菌胺 | 0.5 | GB23200.121 |
氟吡菌酰胺 | 氟吡菌酰胺 | 1 | GB23200.121 |
氟啶胺 | 氟啶胺 | 2 | GB23200.121 |
氟硅唑 | 氟硅唑 | 0.3 | GB 23200.8 |
高效氯氟氰菊酯 | 氯氟氰菊酯(异构体之和) | 0.2 | GB 232008 GB23200.113 |
甲拌磷 | 甲拌磷及其氧类似物(亚砜、砜)之和,以甲拌磷表示 | 0.01 | GB23200.113、GB 23200.116 |
甲霜灵 | 甲霜灵 | 0.2 | GB 23200.113 |
甲氧滴滴涕 | 甲氧滴滴涕 | 0.01 | GB 23200.113 |
精甲霜灵 | 甲霜灵 | 0.2 | GB 23200.113 |
克百威 | 克百威及3G羟基克百威之和,以克百威表示 | 0.02 | GB 23200.112 |
硫丹 | α-硫丹和β-硫丹及硫丹硫酸酯之和 | 0.05 | GB/T 500919 |
六氯苯 | 六氯苯 | 0.10 | 《中华人民共和国药典》2020年版通则0521 |
氯丹 | 顺式氯丹、反式氯丹、氧化氯丹之和 | 0.10 | 《中华人民共和国药典》2020年版通则0521 |
氯氟氰菊酯 | 氯氟氰菊酯(异构体之和) | 0.2 | GB232008 GB23200.113 |
醚菌酯 | 醚菌酯 | 0.1 | GB/T 20769(参见“亚胺菌”) |
嘧菌环胺 | 嘧菌环胺 | 0.2 | GB 23200.113 |
嘧霉胺 | 嘧霉胺 | 1.5 | GB 23200.113 |
七氯 | 七氯、环氧七氯之和 | 0.05 | 《中华人民共和国药典》2020年版通则0521 |
杀虫畏 | 杀虫畏 | 0.01 | GB 23200.113 |
杀扑磷 | 杀扑磷 | 0.05 | GB 23200.113 GB 23200.116 |
霜霉威 | 霜霉威 | 0.5 | GB/T 23211 |
霜霉威盐酸盐 | 霜霉威 | 0.5 | GB/T 23211 |
霜脲氰 | 霜脲氰 | 0.1 | GB/T20769 |
肟菌酯 | 肟菌酯 | 0.03 | GB 23200.8 |
五氯硝基苯 | 五氯硝基苯 | 0.10 | 《中华人民共和国药典》2020年版通则0521 |
戊唑醇 | 戊唑醇 | 0.4 | >GB 23200.113 GB/T20770 |
烯酰吗啉 | 烯酰吗啉 | 0.1 | GB/T 20769 |
乙酰甲胺磷 | 乙酰甲胺磷 | 0.05 | GB 23200.113 GB 23200.116 |
异菌脲 | 异菌脲 | 5 | GB 23200.113、GB 23200.121 |
【标志性成分指标】
应符合表4规定。
表4 标志性成分指标
项目 | 指标 | 检验方法 |
人参皂苷Rg1和人参皂苷Re,% ≥ | 0.30 | 1 皂苷的测定 |
人参皂苷Rb1,% ≥ | 0.20 |
1 皂苷的测定
1.1 仪器与设备
1.1.1 电子分析天平:精度0.1mg。
1.1.2 高效液相色谱仪。
1.1.3 电热恒温水浴锅:±0.5℃。
1.1.4 超声波清洗器:功率≥45W。
1.2 试剂与溶液
1.2.1 乙腈,色谱级纯
1.2.3 三氯甲烷,分析纯
1.2.4 正丁醇,分析纯
1.2.5 甲醇,分析纯
1.3 对照品溶液制备
精密称取人参皂苷Rg1对照品、人参皂苷Re对照品及人参皂苷Rb1对照品,加甲醇制成每lmL各含0.2mg的混合溶液,摇匀,即得。
1.4 色谱条件与系统适用性试验
以十八烷基硅烷键合硅胶为填充剂;以乙腈(色谱级)为流动相A,以水为流动相B,按下表中的规定进行梯度洗脱;检测波长为203nm理论板数按人参皂苷Rgl峰计算应不低于6000。
时间(分钟) | 流动相A(%) | 流动相B(%) |
0~35 | 19 | 81 |
35~55 | 19→29 | 81→71 |
55~70 | 29 | 71 |
70~100 | 29→40 | 71→60 |
1.5 样品的处理
供试品溶液的制备取本品粉末(过四号筛)约1g,精密称定,置索氏提取器中,加三氯甲烷加热回流3小时,弃去三氯甲烷液,药渣挥干溶剂,连同滤纸筒移入100mL锥形瓶中,精密加水饱和正丁醇50mL,密塞,放置过夜,超声处理(功率250W,频率50kHz)30分钟,滤过,弃去初滤液,精密量取续滤液25mL,置蒸发皿中蒸干,残渣加甲醇溶解并转移至5mL量瓶中,加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
1.6 测定
分别精密吸取对照品溶液10μL与供试品溶液10μL,注入液相色谱仪,测定。
1.7 结果
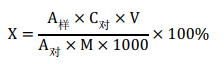
X—样品中人参皂苷的含量,%;
A 样—样品峰面积;
A 对—人参皂苷对照品峰面积;
C 对—人参皂苷对照品溶液浓度,mg/mL
M—样品质量,g;
V—样品溶液总体积,即10mL;
1000—单位换算系数
【储存】应储存在清洁卫生、阴凉干燥(温度不超过20度、相对湿度不高于75%)、通风、防潮、防虫蛀、无异味的库房中,定期检查生晒参的储存情况。
【产品剂型及生产工艺要求】片剂(含片、咀嚼片、口服片)、硬胶囊、软胶囊、粉剂、口服溶液、颗粒剂,茶剂(不含茶叶)
人参原料在产品备案时,允许仅以物理粉碎,或仅经水提取的生产工艺,制成产品时不应再有其他引起物质基础发生改变的生产工艺。
人参粉碎的主要参考工艺为:粉碎、灭菌(一般采取辐照灭菌和湿热灭菌等灭菌方法),干燥(60-70℃),过筛(60-100目)
人参经水提取的主要参考工艺为:粉碎、过筛(10目),水煎2-3次(水量:8-10倍,时间:1-2h),过滤,浓缩
——————————
《保健食品原料目录 西洋参(征求意见稿)》
原料名称 | 每日用量 | 功效 | |||
名称 | 用量范围 | 适宜人群 | 不适宜人群 | 注意事项 | |
西洋参 | 1.5-3g | 易疲劳者 | 少年儿童、孕妇、乳母 湿热体质、阳虚体质者 | 不宜与含有藜芦的中成药同用。 感冒、舌苔厚腻者不推荐使用 | 缓解体力疲劳 |
免疫力低下者 | 增强免疫力 | ||||
西洋参原料技术要求
【来源】
五加科植物西洋参(Panax quinquefolium L.)的干燥根。均系栽培品,秋季采挖,洗净,晒干或低温干燥。
【感官要求】
应符合表1规定。
表 1 感官指标
项目 | 要求 |
色泽 | 全体表面呈浅黄褐色或黄白色。断面浅黄白色。 |
滋味、气味 | 气微而特异,味微苦、甘 |
状态 | 本品呈纺锤形、圆柱形或圆锥形,长3~12cm,直径0.8~2cm。表面可见横向环纹和线形皮孔状突起,并有细密浅纵皱纹和须根痕。主根中下部有一至数条侧根,多已折断。有的上端有根茎(芦头),环节明显,茎痕(芦碗)圆形或半圆形,具不定根(艼)或已折断。体重,质坚实,不易折断。无虫蛀、霉变。 断面平坦,略显粉性,皮部可见黄棕色点状树脂道,形成层环纹棕黄色,木部略呈放射状纹理。 |
【鉴别】
1 显微鉴别
1.1 横切面:木栓层由6-8列切向延长的细胞组成,外部数层细胞常脱落。皮层薄壁细胞10余列,细胞内含草酸钙簇晶,皮层散有树脂道,周围有5-11个分泌细胞。韧皮部树脂道众多,常排列成1-3个同心环,外侧射线中常有裂隙。形成层环明显。木质部导管常单个成2-10个群,径向断续排列,导管木化或微木化,射线细胞1-4列。薄壁细胞含淀粉粒。
1.2 粉末:淡褐色或淡黄白色。树脂道从断面观呈管道状,内含大量金黄色油滴状分泌物和少量橘红色条块状分泌物。草酸钙簇晶较多,直径8-91μm,偏光显微镜下呈亮多彩状。木栓细胞无色、淡黄色或淡黄棕色,类多角形或类方形,垂周壁薄,波状弯曲。导管主要为网纹,梯纹导管,另有环纹及螺纹导管。淀粉粒单粒类圆形至卵形,直径2-28μm,脐点人字形、点状或裂隙状,层纹明显;复粒较少,2-9分粒组成,偏光显微镜下呈黑十字状。
2理化鉴别
取本品粉末lg,加甲醇25mL,加热回流30分钟,滤过,滤液蒸干,残渣加水20mL使溶解,加水饱和的正丁醇振摇提取2次,每次25mL,合并正丁醇提取液,用水洗涤2次,每次10mL>,分取正丁醇液,蒸干,残渣加甲醇4mL使溶解,作为供试品溶液。另取西洋参对照药材lg,同法制成对照药材溶液。再取拟人参皂苷F11对照品、人参皂苷Rb1对照品、人参皂苷Re对照品、人参皂苷Rgl对照品,加甲醇制成每lmL各含2mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述六种溶液各2μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15:40:22:10)5〜10℃放置12小时的下层溶液为展开剂,展开,取出,晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,分别置日光和紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱和对照品色谱相应的位置上,分别显相同颜色的斑点或荧光斑点。
【理化指标】
应符合表2 规定。
表2 理化指标
项目 | 指标 | 检测方法 |
水分,% ≤ | 13.0 | GB 5009.3 |
灰分,% ≤ | 5.0 | GB 5009.4 |
铅(以Pb计),mg/kg ≤ | 2.0 | GB 5009.12 |
总砷(以As计),mg/kg ≤ | 1.0 | GB5009.11 |
总汞(以Hg计),mg/kg ≤ | 0.2 | GB 5009.17 |
镉(以Cd计), mg/kg ≤ | 1.0 | GB 5009.15 |
铜(以Cu计),mg/kg ≤ | 20 | GB 5009.13 |
【农药残留】
应符合表3规定。
表3 农药残留指标
农药名称 | 残留物 | 最大残留量mg/kg | 检测方法 |
苯醚甲环唑 | 苯醚甲环唑 | 0.5 | GB 23200.113 |
丙环唑 | 丙环唑 | 0.1 | GB 23200.113 |
甲霜灵 | 甲霜灵 | 0.2 | GB 23200.113 |
氯氟氰菊酯 | 氯氟氰菊酯(异构体之和) | 0.2 | GB 232008、GB23200.113 |
嘧霉胺 | 嘧霉胺 | 1.5 | GB 23200.113 |
杀扑磷 | 杀扑磷 | 0.05 | GB 23200.113、GB 23200.116 |
戊唑醇 | 戊唑醇 | 0.4 | GB 23200.113、GB/T 20770 |
烯酰吗啉 | 烯酰吗啉 | 0.1 | GB /T20769 |
硫丹 | α-硫丹和β-硫丹及硫丹硫酸酯之和 | 0.05 | GB/T 500919 |
七氯 | 七氯、环氧七氯之和 | 0.05 | 《中华人民共和国药典》2020年版通则0521 |
五氯硝基苯 | 五氯硝基苯 | 0.10 | 《中华人民共和国药典》2020年版通则0521 |
六氯苯 | 六氯苯 | 0.10 | 《中华人民共和国药典》2020年版通则0521 |
氯丹 | 顺式氯丹、反式氯丹、氧化氯丹之和 | 0.10 | 《中华人民共和国药典》2020年版通则0521 |
六六六 | α-六六六、β-六六六,γ-六六六,六、γ-六六六和δ-六六六之和,以六六六表示 | 0.1 | 《中华人民共和国药典》2020年版通则 |
滴滴涕 | 4,4'-滴滴涕、2,4'-滴滴涕、4,4'-滴滴伊、4,4'-滴滴滴之和,以滴滴涕表示 | 《中华人民共和国药典》2020年版通则 |
【标志性成分指标】
应符合表4规定。
表4 标志性成分指标
项目 | 指标 | 检验方法 |
人参皂苷Rg1、人参皂苷Re和人参皂苷Rb1,% ≥ | 2.0 | 1 皂苷的测定 |
1 皂苷的测定
1.1 仪器与设备
1.1.1 电子分析天平:精度0.1mg。
1.1.2 高效液相色谱仪。
1.1.3 电热恒温水浴锅:±0.5℃。
1.1.4 超声波清洗器:功率≥45W。
1.2 试剂与溶液
1.2.1 乙腈,色谱级纯
1.2.3 磷酸,分析纯
1.2.4 正丁醇,分析纯
1.2.5 甲醇,分析纯
1.3 对照品溶液制备
准确称取人参皂苷Rg1对照品、人参皂苷Re对照品及人参皂苷Rb1对照品,加甲醇制成每lmL各含人参皂苷Rg10.1mg、人参皂苷Re0.4mg及人参皂苷Rb11mg 的混合溶液,摇匀,即得。
1.4 色谱条件与系统适用性试验
以十八烷基硅烷键合硅胶为填充剂;以乙腈(色谱级)为流动相A,以0.1%磷酸溶液为流动相B,按下表中的规定进行梯度洗脱;检测波长为203nm;柱温40℃。理论板数按人参皂苷Rbl峰计算应不低于5000。
时间(分钟) | 流动相A(%>) | 流动相B(%) |
0~25 | 19→20 | 81→80 |
25~60 | 20→40 | 80→60 |
60~90 | 40→55 | 60→45 |
90~100 | 55→60 | 45→40 |
1.5 样品的处理
准确称取本品粉末(过三号筛)约1g,精密称定,置具塞锥形瓶中,精密加入水饱和的正丁醇50mL,称定重量,置水浴中加热回流提取1.5小时,放冷,再称定重量,用水饱和正丁醇补足减失的重量,摇匀,滤过。精密量取续滤液25mL,置蒸发皿中,蒸干,残渣加50%甲醇适量使溶解,转移至10mL量瓶中,加50%甲醇至刻度,摇匀,滤过,取续滤液,即得。
1.6 测定
分别精密吸取对照品溶液10μL与供试品溶液10μL,注入液相色谱仪,测定。
1.7 结果
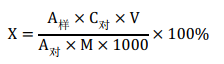
X—样品中人参皂苷的含量,%;
A 样—样品峰面积;
A 对—人参皂苷对照品峰面积;
C 对—人参皂苷对照品溶液浓度,mg/mL
M—样品质量,g;
V—样品溶液总体积,即10mL;
1000—单位换算系数
【储存】成品西洋参应储存在清洁卫生、阴凉干燥(温度不超过20度、相对湿度不高于75%)、通风、防潮、防虫蛀、无异味的库房中,定期检查西洋参的储存情况。
【产品剂型及生产工艺要求】片剂(含片、咀嚼片、口服片)、硬胶囊、软胶囊、粉剂、口服溶液、颗粒剂,茶剂(不含茶叶)
西洋参原料在产品备案时,允许仅以物理粉碎,或仅经水提取的生产工艺,制成产品时不应再有其他引起物质基础发生改变的生产工艺。
西洋参粉碎的参考主要工艺为:粉碎、灭菌(一般采取辐照灭菌和湿热灭菌等灭菌方法),干燥(60-70℃),过筛(60-100目)
人参经水提取的主要参考工艺为:粉碎、过筛(10目),水煎2-3次(水量:8-10倍,时间:1-2h),过滤,浓缩,干燥
——————————
《保健食品原料目录 灵芝(征求意见稿)》
原料名称 | 每日用量 | 功效 | |||
名称 | 用量范围 | 适宜人群 | 不适宜人群 | 注意事项 | |
灵芝 | 4-6g | 免疫力低下者 | 少年儿童、孕妇、乳母 | 增强免疫力 | |
灵芝原料技术要求
【来源】
多孔菌科真菌赤芝(Ganoderma lucidum (Leyss. ex Fr.) Karst.)、紫芝(Ganoderma sinense Zhao, Xu et Zhang)的干燥子实体。除去杂质,剪除附有朽木、泥沙或培养基质的下端菌柄,阴干或40~50℃烘干而得。
【感官要求】
应符合表1 规定。
表1 感官指标
项目 | 要求 |
色泽 | 全体表面呈浅黄褐色或黄白色。断面浅黄白色。 |
滋味、气味 | 气微而特异,味微苦、甘 |
状态 | 赤芝:外形呈伞状,菌盖肾形、半圆形或近圆形,直径10~18cm,厚1~2cm。皮壳坚硬,黄褐色至红褐色,有光泽,具环状棱纹和辐射状皱纹,边缘薄而平截,常稍内卷。菌肉白色至淡棕色。菌柄圆柱形,侧生,少偏生,长7~15cm,直径1~3.5cm,红褐色至紫褐色,光亮。孢子细小,黄褐色。 紫芝:皮壳紫黑色,有漆样光泽。菌肉锈褐色。菌柄长17~23cm。 栽培品子实体较粗壮、肥厚,直径12~22cm,厚1.5~4cm。皮壳外常被有大量粉尘样的黄褐色孢子。 |
【鉴别】
1 本品粉末浅棕色、棕褐色至紫褐色。菌丝散在或粘结成团,无色或淡棕色,细长,稍弯曲,有分枝,直径2.5~6.5μm。孢子褐色,卵形,顶端平截,外壁无色,内壁有疣状突起,长8~12μm,宽5~8μm。
2 取本品粉末2g,加乙醇30mL,加热回流30min,滤过,滤液蒸干,残渣加甲醇2mL使溶解,作为供试品溶液。另取灵芝子实体对照药材2g,同法制成对照药材溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各4μl,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-甲酸乙酯-甲酸(15:5:1)的上层溶液为展开剂,展开,取出,晾干,置紫外光灯(365nm)下检视。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的荧光斑点。
3 取本品粉末1g,加水50mL,加热回流1小时,趁热滤过,滤液置蒸发皿中,用少量水分次洗涤容器,合并洗液并入蒸发皿中,置水浴上蒸干,残渣用水5mL溶解,置50mL离心管中,缓缓加入乙醇25mL,不断搅拌,静置1h,离心(转速为每分钟4000转),取沉淀物,用乙醇10mL洗涤,离心,取沉淀物,烘干,放冷,加4mol/L 三氟乙酸溶液2mL,置10mL安瓿瓶或顶空瓶中,封口,混匀,在120℃水解3h,放冷,水解液转移至50mL烧瓶中,用2mL水洗涤容器,洗涤液并入烧瓶中,60℃减压蒸干,用70%乙醇2mL溶解,置离心管中,离心,取上清液作为供试品溶液。另取半乳糖对照品、葡萄糖对照品、甘露糖对照品和木糖对照品适量,精密称定,加70%乙醇制成每1mL各含0.1mg的混合溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各3μl,分别点于同一高效硅胶G薄层板上,以正丁醇-丙酮-水(5:1:1)为展开剂,展开,取出,晾干,喷以对氨基苯甲酸溶液(取4-氨基苯甲酸0.5g,溶于冰醋酸9mL中,加水10mL和85%磷酸溶液0.5mL,混匀),在105℃加热10分钟,置紫外光灯(365nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。其中最强荧光斑点为葡萄糖,甘露糖和半乳糖荧光斑点强度相近,位于葡萄糖斑点上、下两侧,木糖斑点在甘露糖上,荧光斑点强度最弱。
【理化指标】
应符合表2 规定。
表2 理化指标
项目 | 指标 | 检测方法 |
水分,% ≤ | 17.0 | GB 5009.3 |
灰分,% ≤ | 3.2 | GB 5009.4 |
铅(以Pb计),mg/kg ≤ | 1.0 | GB 5009.12 |
总砷(以As计),mg/kg ≤ | 0.5 | GB5009.11 |
总汞(以Hg计),mg/kg ≤ | 0.1 | GB 5009.17 |
镉(以Cd计), mg/kg ≤ | 0.2 | GB 5009.15 |
【农药残留】
应符合表3规定。
表3 农药残留指标
农药名称 | 残留物 | 最大残留量 mg/kg | 检测方法 |
丁硫克百威 | 丁硫克百威 | 0.01 | GB 23200.13 |
乐果 | 乐果 | 0.01 | GB 23200.113、GB 23200.116、GB/T 5009.145、GB/T 20769、 |
硫丹 | α-硫丹和β-硫丹及硫丹硫酸酯之和 | 0.05 | GB/T5009.19 |
杀扑磷 | 杀扑磷 | 0.05 | GB 23200.8、GB 23200.113、GB 23200.116、GB/T 4553、 |
乙酰甲胺磷 | 乙酰甲胺磷 | 0.05 | GB 23200.113、GB 23200.116、GB/T 5009.103、GB/T 5009.145 |
特丁硫磷 | 特丁硫磷及其氧类似物(亚砜、砜)之和,以特丁硫磷表示。 | 0.01 | SN/T 4591 |
三氯沙螨醇 | 三氯沙螨醇(o,p'-异构体和p,p'-异构体之和 | 0.01 | GB 23200.110、GB/T 5009.176 |
【标志性成分指标】
应符合表4规定。
表4 标志性成分指标
项目 | 指标 | 检验方法 |
多糖,% ≥ | 0.90(以无水葡萄糖(C6H12O6)计) | 1 多糖的测定 |
三萜及甾醇,% ≥ | 0.50 (以齐墩果酸(C30H48O3)计) | 2 三萜及甾醇的测定 |
1 多糖的测定
1.1 仪器与设备
1.1.1 电子分析天平:精度0.1mg。
1.1.2 紫外可见分光光度计:±2nm。
1.1.3 电热恒温水浴锅:±0.5℃。
1.1.4 离心机:(0-4000)rpm/min。
1.2 对照品溶液制备
葡萄糖对照品的配制:准确称取干燥至恒重的葡萄糖对照品适量,精密称定,加水制成每1mL含0.12mg的溶液,即得。
硫酸蒽酮溶液的制备(临用现配):准确称取0.1g蒽酮置于烧杯中,缓缓加入100mL硫酸溶解,摇匀,即得。
1.3 标准曲线的绘制
分别精密量取葡萄糖对照品溶液0.2mL、0.4mL、0.6mL、0.8mL、1.0mL、1.2mL,分别置于具塞试管中,补充水至2.0mL,加入硫酸蒽酮溶液6mL,立即摇匀,放置15min后,立即置冰浴中冷却15min,取出,以相应的试剂为空白,用紫外可见分光光度计在625nm波长处测定吸光度。以葡萄糖质量为横坐标,吸光度值为纵坐标,绘制标准曲线。
1.4 样品的处理
取本品粉末约2g,精密称定,置圆底烧瓶中,加水60mL静置1小时,加热回流4h,趁热滤过,用少量热水洗涤滤器和滤渣,将滤渣及滤纸置烧瓶中,加水60mL,加热回流3h,趁热滤过,合并滤液,置水浴上蒸干,残渣用水5mL溶解,边搅拌边缓慢滴加乙醇75mL,摇匀,在4℃放置12h,离心,弃去上清液,沉淀物用热水溶解并转移至50mL量瓶中,放冷,加水至刻度,摇匀,取溶液适量,离心,精密量取上清液3mL,置25mL量瓶中,加水至刻度,摇匀,即得。
1.5 精密量取供试品溶液2mL,置具塞试管中,照标准曲线制备项下的方法,自“迅速精密加入硫酸蔥酮溶液6mL”起,同法操作,测定吸光度,从标准曲线上读出供试品溶液中无水葡萄糖的含量,计算,即得。
1.7 结果
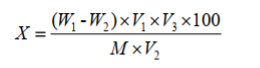
X—样品中多糖含量(以葡萄糖计),mg/100g;
W1—从标准曲线上查得样品测定液中含粗多糖的质量,mg;
W2—从标准曲线上查得样品空白液中含粗多糖的质量,mg;
M—样品质量,g;
V1—样品沉淀物定容体积,mL;
V2—移取沉淀物溶液量,mL;
V3—移取液稀释体积,mL;
100—单位换算系数。
2 三萜及甾醇的测定
2.1 仪器与设备
2.1.1 电子分析天平:精度0.1mg。
2.1.2 紫外可见分光光度计:±2nm。
2.1.3 超声波清洗器:功率≥45W。
2.1.4 电热恒温水浴锅:±0.5℃。
2.2 试剂与溶液
2.2.1 高氯酸,分析纯。
2.2.4 冰醋酸,分析纯。
2.2.5 香草醛,分析纯。
2.2.6 乙酸乙酯,分析纯。
2.3 对照品溶液制备
齐墩果酸对照品的配制:取齐墩果酸对照品(纯度≥98%)适量,精密称定,加甲醇制成每1mL含0.2mg的溶液,即得。
香草醛冰醋酸溶液(临用现配):精密称取香草醛0.5g,加冰醋酸使溶解成10mL,即得。
2.4 标准曲线的绘制
精密量取对照品溶液0.1、0.2、0.3、0.4、0.5mL,分别置15mL具塞试管中,挥干,放冷,精密加入新配制的香草醛冰醋酸溶液0.2mL,高氯酸0.8mL,摇匀,在70℃水浴中加热15min,立即置冰浴中冷却5分钟,取出,精密加入乙酸乙酯4mL,摇匀。用分光光度计于
546nm波长处测定吸光度,以吸光度为纵坐标、浓度为横坐标绘制标准曲线。
2.5 样品的处理
取本品粉末约2g,精密称定,置具塞锥形瓶中,加乙醇50mL,超声处理(功率140W,频率42kHz)45分钟,滤过,滤液置100mL量瓶中,用适量乙醇,分次洗涤滤器和滤渣,洗液并入同一量瓶中,加乙醇至刻度,摇匀,即得。
2.6 样品的测定
精密量取供试品溶液0.2mL,置15mL具塞试管中,照标准曲线制备项下的方法,自“挥干”起,同法操作,测定吸光度,从标准曲线上读出供试品溶液中齐墩果酸的含量,计算,即得。
2.7 结果
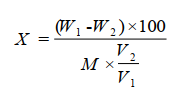
X—样品中三萜及甾醇含量(以齐墩果酸计),mg/100g;
W1—从曲线上查得样品测定液中含三萜及甾醇的质量,mg;
W2—从曲线上查得样品空白液中含三萜及甾醇的质量,mg;
M—样品质量,g;
V1—样品测定液总体积,mL;
V2—比色测定时所移取样品测定液的体积,mL。
【储存】存放于通风、干燥、阴凉的仓库内,严禁与有害、有异味、有腐蚀性的物品混贮,
堆放须隔墙离地。防霉,防蛀。
【产品剂型及生产工艺要求】片剂(含片、咀嚼片、口服片)、硬胶囊、软胶囊、粉剂、口服溶液、颗粒剂,茶剂(不含茶叶)
灵芝原料在产品备案时,允许仅以物理粉碎,或仅经水提取,制成产品时不应再有其他引起物质基础发生改变的生产工艺。
灵芝打粉的主要参考工艺为:粉碎、灭菌(一般采取湿热灭菌等灭菌方法),干燥,过筛(80-100目)
灵芝经水提取的主要参考工艺为:粉碎、过筛(10目),水煎2-3次(水量:10-12倍,时间:1-2h),过滤(200目),浓缩,干燥
——————————











 沪ICP备11012790号
沪ICP备11012790号 沪公网安备31010702005226号
沪公网安备31010702005226号 上海工商
上海工商